
手机扫码访问本站

微信咨询
克里唑替尼(亦翻译为:克唑替尼)是FDA批准的首个非小细胞肺癌精准药物,也是肿瘤药物研发史上开发最快的四大传奇药物之一。2006年,克里唑替尼被发现对携带EML4-ALK融合基因表达的肿瘤细胞具有抑制作用,并开始I期临床试验,2011年克里唑替尼通过快速通道被FDA批准上市,并引发轰动,主导发明人华裔女科学家崔景荣博士也因此荣获第38届美国国家发明者年度奖,每年全美各行业中只有一个专利可获此殊荣。
克里唑替尼的研发历程既有偶然的成分也有必然的成分,偶然的是克里唑替尼本是基于c-Met激酶结构进行设计的,却对ALK激酶具有强效的抑制活性,而必然的是由苗头化合物向先导化合物过度时是依据传统的药物化学和构效关系为策略进行的,同时利用复合物晶体结构对结构进行“量体裁衣”式的优化,后期则用亲亲脂性效率对成药性进行全程“监视”。“变幻莫测”却“有的放矢”就是科学的魅力所在。
辉瑞研发的舒尼替尼于2006年上市,该药对多种酪氨酸激酶均有较强的抑制活性,故可用于治疗对伊马替尼耐药的胃肠道间质瘤患者。循此研发路径,辉瑞继续着手研发与其他激酶有关的肿瘤药物。间充质上皮转化因子激酶 (c-Met) 也是受体酪氨酸激酶,其信号通路对发育、器官形成和机体稳态起着重要作用,因此c-Met被认为是肿瘤药物治疗的重要靶标。
考虑到羟基吲哚的N-H和C=O结构可与激酶通过氢键结合,故辉瑞对具有羟基吲哚结构的化合物进行筛选发现,衍生物1对c-Met激酶具有较强的抑制活性(IC50=10 nmol·L-1),且在1μmol·L-1浓度下可因抑制c-Met而完全阻止A549细胞的生长,故认为衍生物1具有较好的开发潜能。
为了提高该衍生物对c-Met激酶的选择性,研究人员分别在母核的4位或5位分别引入取代苯基和苄基磺酰基侧链,设计并合成了一系列衍生物。

对合成近千个化合物进行活性测定发现,衍生物4对c-Met激酶具有较高的选择性,强于对其他激酶抑制活性的50倍以上,且对c-Met激酶的抑制活性亦较高(IC50=9 nmol·L-1);体内实验表明,化合物4能抑制移植性肿瘤细胞的c-Met磷酸化,其活性参数测定结果为:配体效率LE=0.25、亲脂性效率LipE=4.85、分布系数logD=3.20,故化合物4可作为候选化合物进入开发阶段。
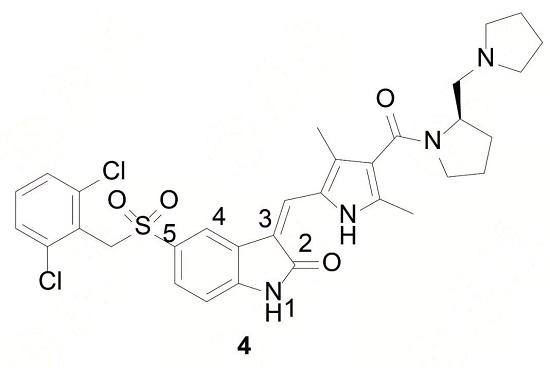
通过对化合物4与c-Met激酶的复合物晶体结构分析发现:(1) 结合域的 A-环套采取了独特的自身抑制状态的构象,即在激酶的活化环套残基1222~1227形成转折,占据了αC螺旋的催化位置,使得1228~1245环套残基移位,干扰了ATP 与底物的结合;(2) 吲哚酮的N-H和C=O基团与激酶的残基分别形成氢键;(3) 吲哚酮的C=O与吡咯环的N-H形成分子内氢键,因而吲哚酮与吡咯环形成较大的共轭平面,处于ATP的腺嘌呤环结合的平面裂隙处;(4) 连接羟基吲哚与二氯苯基的连接基磺酰亚甲基形成U-形转折,使二氯代苄基与具有独特构象的A-环套上Tyr1230的苯酚环发生π-π堆积作用;(5) 磺酰基的氧原子与 Asp1222的N-H形成氢键,稳定了分子取向;(6) 与吡咯环相连的酰胺及延伸的片段进入了水相,未与蛋白结合。
从结合信息可知,二氯苯基为了可与Tyr-1230发生π-π堆积作用,磺酰亚甲基自行进行U-形转折,可能是由于二氯苯基、吲哚酮及吡咯环形成的共轭平面过大,故需缩小其基本骨架。基于骨架跃迁原理,首先将吲哚酮与吡咯的分子内氢键“固化”成共价键,为氮杂吖啶5;随后切断C-N键形成2-氨基-3-苯基吡啶化合物6;最后进一步简化连接基团,得到衍生物7。

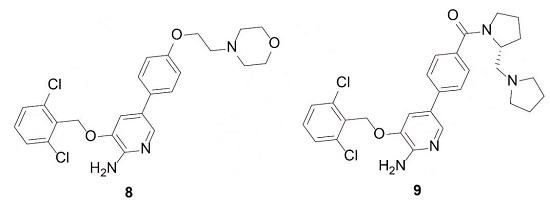
虽然衍生物7对c-Met激酶的抑制活性较弱Ki=3.83μmol·L-1,但是由于分子量比较低,其配体效率优于5(LE=0.29),但亲脂性效率有所降低(LipE=0.35)。故可在衍生物苯环的羟基处引入极性侧链,引入吗啉亚乙基得到衍生物8,活性略有提高(Ki=2.45 μmol·L-1),但是降低了配体率,随后模仿衍生物4的片段,得到9,抑制活性和亲脂性效率均有所提高,Ki=0.46μmol·L-1,LE=0.24,LipE=3.70。
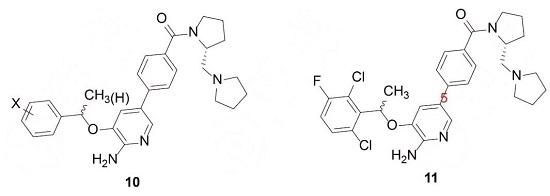
为了考察环上取代基对活性Ki和亲脂性效率LipE的影响,在苯环上引入一个或多个、相同或不同的卤素,连接链或用甲基取代、或不取代,合成了一系列通式10的衍生物,活性测定发现,衍生物11的活性最高,对c-Met酶的活性参数为:Ki=0.012μmol·L-1、LipE=4.82;对c-Met细胞的活性参数为:IC50=0.020μmol·L-1、 LipE=4.60。
根据复合物的晶体结构,5-苯基结合于Tyr1159、Ile1084和Gly1163构成的疏水性狭窄裂隙,这需要确保在氨基吡啶的5位连接的芳环具有平面性,芳基上连接的基团延伸到溶剂相中。此外,11中的酰胺片段已离开疏水裂隙,进入水相,提示延伸的亲水性片段可不必经酰胺键连接。
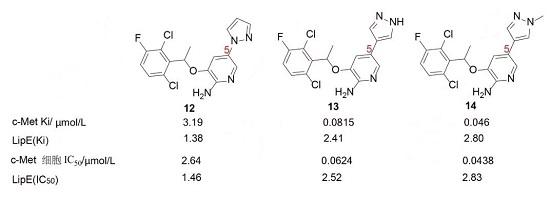
用五元含氮芳环替换5-苯环可增加水溶性,例如含5-吡唑或咪唑化合物的 cLogD比相应的苯化合物低2个单位,并且较小扭角,增加了共面性,有利于结合。氨基吡啶与吡唑环的连接方式对活性影响很大,例如化合物12和13的活性以及 LipE 值相差很大。结构生物学表明,12的吡唑环氮原子所处的位置使得c-Met的残基Met1160和Ile1084取向与吡唑环邻近,不利于氨基吡啶的氢键结合,而且该吡唑环处于酶蛋白的疏水性界面,为了发生疏水-疏水相互作用,N原子的孤电子对的去水合作用是不利的焓变;而13的N原子都进入了水相,没有上述的不利效应,因而活性高12,酶或细胞活性提高了30~40倍。化合物13的N-甲基化后产14的活性更强,提示由这个N原子可引出含有极性基团的碳链,以提高活性水溶性。
鉴于化合物9结构中含有延伸到水相的碱性基团能够提高活性和亲脂性效率,因而也在吡咯环系上引入尽可能小的碱性片段,例如链烷基,胺、氮杂环丁烷、四氢吡咯、哌啶等,以增加活性和改善药学和药代性质。在选择高活性和高亲脂性效率的化合物同时,还评价对人肝微粒体的稳定性,从有代表性的化合物中优选出15和16,尤其是因16的高活性和较好的代谢稳定性,确定为候选药物。
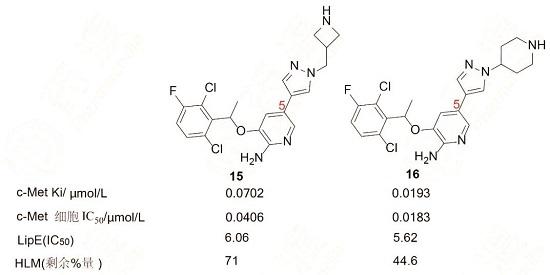
前述优化过程制备的吡唑系列化合物含有手性碳原子,都是用混旋的样品测定活性的。将优选出的化合物16拆分成光学活性物质,活性测定表明,R-构型的分17活性强于RS和S构型,对酶和细胞抑制活性分别为Ki = 0.002μmol·L-1和IC50=0.008μmol·L-1,命名为克里唑替尼(crizotinib)。
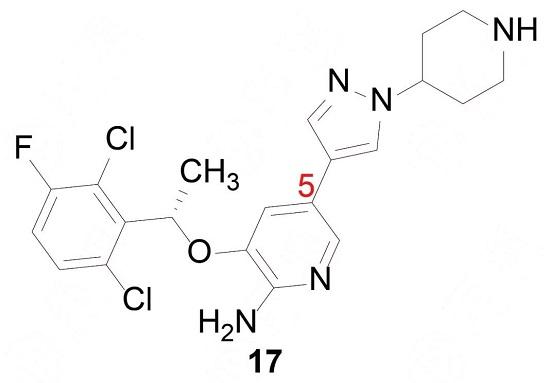
克里唑替尼从2007年立项到2011年FDA批准上市,仅用了4年时间,它的出现是个体化治疗的又一重大突破,其在临床上的地位超越了常规化疗,是当前ALK 阳性的晚期非小细胞肺癌患者标准药物。
1 Cui JR, et al. 4-Aryl substituted indolinones. WO02/055517
2 Cui JR, et al. 5-Aralkylsulfonyl-3-(pyrrol-2-ylmethylidene)-2-indolinones as kinaseinhibitors. WO 02/096361
3 Cui JR, Tran DM, Shen H, et al. Structurebased drug design of crizotinib (PF-02341066), a potent and selective dualinhibitor of mesenchymal-epithelial transition factor (c-MET) kinase andanaplastic lymphoma kinase (ALK). J Med Chem, 2011, 54: 6342-6363
4 Roberts PJ. Clinical use of crizotinib for thetreatment of non-small cell lung cancer. Biologics, 2013, 7: 91–101.