
手机扫码访问本站

微信咨询
氯化铁,黑棕色六方晶系结晶。在透射光线下呈石榴红色,反射光线下呈金属绿色。 易溶于水、甲醇、乙醇、丙酮和乙醚。溶于液体二氧化硫、三溴化磷、三氯氧磷、乙胺、苯胺,微溶于二硫化碳,不溶于甘油。三氯化铁有腐蚀性。其粉尘能刺激黏膜引起炎症。生产操作人员和装卸搬运人员要穿工作服、橡皮围裙,戴乳胶手套等劳保用品,防止与皮肤接触。生产设备要密闭,车间通风良好。
方法一[2]:应用硫铁矿烧渣生产液体三氯化铁,经过反应、沉清、氧化、蒸发等工艺,制得液体三氯化铁,产品符合GB/T1621-93工业氯化铁标准。此法具有工艺条件温和,操作方法简单,容易形成规模生产等优点,特别适宜于硫铁矿与制酸厂生产。工艺流程示意图如下。
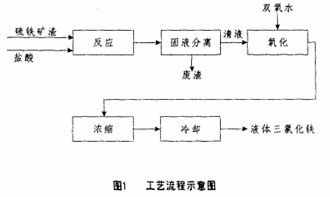
这个过程反应原理为硫铁矿渣具有三种形态的氧化物,分别是 FeO、Fe3O4、Fe2O3、其中FeO为 0.5%左右,其余的是Fe3O4、Fe2O3,它们与盐酸的反应式如下所示:
FeO+2HCl=FeCl2+H2O
Fe3O4+8HCl=2FeCl3+FeCl2+4H2O
Fe2O3+6HCl=2FeCl3+3H2O
反应后的液体三氯化铁中还存在少量的FeCl2用双氧水氧化成FeCl3,反应方程式如下所示:
2FeCl2+H2O2+2HCl=2FeCl3+2H2O
具体的反应及控制过程如下:将4吨30%的盐酸加入5000L的搪玻璃反应釜内,然后一边搅拌一边加入矿渣1.665吨(含铁50%),矿渣与盐酸的质量比为0.4~0.45:1,由于反应为放热反应,随着反应的进行,温度不断上升,而温度上升使得反应速度加快,所以反应过程的温度不用控制,让其自然地升高,最高温度可以达到98℃左右,反应时间大概为1h,反应完成控制游离酸含量 约为2%。
控制游离酸含量较高是为了下一步的氧化提供有利的反应条件。固液分离过程将反应釜内的物料放入到上部圆形下部锥形内衬瓷板的沉清池内进行沉清,大概8个小时后,再放出上层棕色的清液到储液池,再加清水洗渣,沉清后的清液再放到储液池,底部残渣用水冲洗,排到废水处理池沉淀分离。
氧化过程是将分离出的清液在常温下用泵送入到混合器与双氧水(含量27.5%)混合,再根据清液中所含的氯化亚铁的量来调整双氧水的加入量,一般而言是每吨成品加入50kg,最后再来测定氯化亚铁含量,要控制氯化亚铁含量小于等于0.25%,然后经过氧化处理的清液放入储液罐。
最后一步过程是浓缩和冷却过程,氧化后的料液要用泵送入到10000L搪玻璃反应锅内,再用石墨加热器来加热蒸发水分,石墨加热器内的蒸汽压力应控制小于等于0.4Mpa,蒸发终点以测定浓度来控制,当料液温度达到115℃左右取样检测浓度,当三氯化铁含量达到38%时,放料到冷却池,自然冷却到温度小于等于40℃,就得到了液体三氯化铁成品。
方法二[3]:盐酸酸洗废液制备三氯化铁,通过在盐酸酸洗废液中加入适量的铁屑和盐酸 ,调整料液中氯化亚铁与盐酸含量的比例 ,使氯化亚铁在酸性介质下与中性催化剂的作 用 ,直接与氧气应生成三氯化铁。反应方程式为:
2HCl+Fe = FeCl2+ H2
4HCl+ 4FeCl2+ O2=4FeCl3+ 2H2O
盐酸酸洗废液制备三氯化铁工艺流程图如下所示 。
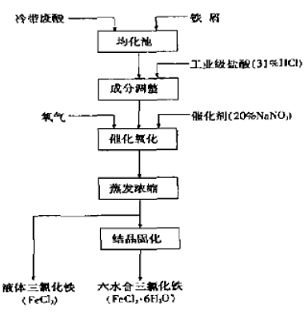
将适量的铁屑放人均化池中,再注入盐酸废液,任其自然反应,制得中间产品氯化亚铁溶液,然后通过过滤器,滤去杂质,清液进入成分调整池,在调整池中再加人工业级酸(31%HCl) ,并使料的氯化亚铁与盐酸的比例为3.5 :1。接着进行催化氧化过程。
将调整好的料液泵人反应罐中,通人氧气驱除罐中液面上的空气 (约 1kgO2) 密闭反应系统,向反应罐套层通蒸汽加热至 50~60℃,同时,缓缓加入适量的催化剂亚硝酸钠和氧气,罐中料液开始发生催化反应,反应速度不断加快, 当反应物料温度开至65—70℃时 ,停止蒸汽加热 和暂停加催化剂,并加大氧气量,控制反应罐内压力为0~2kPa ,氧化反应处于加速状态,随后,适时添加催化剂,经约3小时,氧化反应处于终结 ,取样化验,FeCl2< 04g/L 时 ,即告氧化反应结束 ,反应物便可转入蒸发浓缩罐。最后进行蒸发浓缩。
将反应罐中的三氯化铁液体初始产物泵入蒸发罐中,通蒸汽于夹层内加 热,同时,启动冷凝器和水环真空泵,在 加热减压的条件下,使物料维持沸腾蒸发状态。 随着不断蒸发浓缩,物体的沸腾温度也不断升高 ,适时控制蒸发浓缩条件,便可分别制得工业级一、二 、三 类液体三氯化铁产品(浓度分别为39%、41%、45%) ,最终获得六水合三氯化铁固态 (FeCl3·6H2O) 产品。
氯化铁主要用作饮水的净水剂和废水的处理净化沉淀剂。印染工业用作靛蓝染料染色时的氧化剂和印染媒染剂。有机合成二氯乙烷等生产的催化剂。银矿和铜矿的氯化浸提剂。照相和印刷制版的刻蚀剂。制造磷酸铁等铁盐、医药、颜料和墨水的原料。在建筑混凝土中渗入其溶液后能增加建筑物强度、抗腐蚀性和防止渗水。用于电子工业线路板及荧光数字筒生产。生产肥皂的废液回收甘油时的凝聚剂。
此外主要用作工业水处理、照相和印刷制版的腐蚀剂、有机合成工业的催化剂、氧化剂,染料工业的氧化剂和媒染剂制造其它铁盐、颜料、墨水、医药的原料等 高纯级(99.99%)在氢作用下和金属卤化物气相共还原产生可分离的金属间化合物,该化合物具有导热导电、磁感应和抗氧化特性。
[1] 化学教材研究中心.化学选修4.北京:人民教育出版社,2010.
[2]李春华. 用硫铁矿烧渣生产液体三氯化铁新工艺[J]. 广东化工, 2004, 31(5):5-5.
[3]龙松贞. 盐酸酸洗废液制备三氯化铁新工艺的探讨[J]. 涟钢科技与管理, 2000(2):57-59.
[4] 北京师范大学、华中师范大学、南京师范大学无机化学教研室.无机化学.北京:高等教育出版社,2003:772-772