
手机扫码访问本站

微信咨询
碳酸镁是一种含镁元素的白色粉末状,呈弱碱性的无机化合物。碳酸镁的化学性质稳定,无毒无味,不可燃。与酸性比碳酸强的酸发生复分解反应生成盐和二氧化碳等多种物质,微溶于水、丙酮和液氨。具有吸水和吸油性,因此体操、举重和攀岩运动员常常利用俗称“镁粉”的碳酸镁擦手以保持双手干燥,但碳酸镁可能令某些人皮肤过敏。此外,碳酸镁还可作为制酸剂、便秘药等肠胃相关药品。

碳酸镁性状为白色至黄色的固体结晶或晶体粉末。能耐高温且难溶于水、丙酮和液氨,但易溶于铵盐水溶液。
将碳酸镁加热到250℃至800℃,会分解为氧化镁和二氧化碳,这个过程被称为煆烧:
MgCO3→ MgO + CO2
盐酸
碳酸镁与盐酸反应,生成氯化镁、水和二氧化碳
MgCO3+2HCl → MgCl2+H2O+CO2↑
硫酸
碳酸镁与硫酸反应,会生成硫酸镁、水和二氧化碳:
MgCO3+ H2SO4→ MgSO4+ CO2+ H2O
碳酸镁通常是通过采掘菱镁矿获得,而三水合碳酸镁MgCO3·3H2O可通过混合镁溶液和碳酸根溶液获得,其中碳酸根来源可以是大气中的二氧化碳。碳酸镁还可以通过如下方法制备:氢氧化镁悬浊液置于3.5-5倍大气压的二氧化碳氛围中加热至50℃,得到可溶的碳酸氢镁:
Mg(OH)2+ 2 CO2→ Mg(HCO3)2
然后将混合液过滤,滤液在真空干燥下得到含有碳酸镁的水溶液:
Mg2++ 2 HCO3-→ MgCO3+ CO2+ H2O
苦卤与碱反应制碳酸镁反应式:
5 MgCl2+ 5 Na2CO3+ 5 H2O → 4MgCO3·Mg(OH)2·4H2O + 10 NaCl + CO2
5 MgSO4+ 5 Na2CO3+ 7 H2O → 4MgCO3·Mg(OH)2·6H2O + 5 Na2SO4+ CO2
碳酸和氢氧化镁混合反应式:
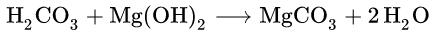
碳酸镁主要有以下用途:
作为干燥剂或吸水、食物添加剂(胡椒粉)、胃药和泻药;
用于制备化学试剂、橡胶填料和防火涂料;
用于制备二氧化碳和氧化镁;
用于制备硫酸镁、氯化镁和水。
虽然碳酸镁本身不具毒性,不过一些人可能对其过敏。长期或过量地使用和接触,可能会影响中枢神经系统、患上抑郁症和心脏功能紊乱。如果不慎接触眼睛或吸入,会刺激眼睛、呼吸道和消化道,长期吸入更会引发肺尘病。