
手机扫码访问本站

微信咨询
硫化亚铜(Cu2S ),是一种P型窄禁带半导体材料,其禁带宽度约为1.2eV。硫化亚铜具有多种晶型结构,目前发现已经有单斜晶系、六方晶系和立方晶系等。其中,常见的辉铜矿Cu2S具有相变特性。当温度低于101.5 ℃(纳米线)或103.5 ℃(块材)时,称为,相Cu2S (低温单斜晶结构,也称低辉铜矿),当温度高于101.5 ℃(纳米线)或103.5 ℃(块材)时,表现为刀相(高温六方晶系结构,也称高辉铜矿)。这两种结构都能够稳定存在。高辉铜矿属于P63/mmc空间群,每个晶胞拥有2个硫原子和4个铜原子。硫原子占据了六方点格,铜原子随机的占据了一些高对称威科夫位。铜原子的亚晶格特点使高辉铜矿表现出固溶体(合金)的特征。对于低辉铜矿,每个晶胞拥有96个硫原子和192个铜原子,但是每个铜原子占据一个特定的位置。因此,辉铜矿Cu2S的相变表现往往被认为是从晶体到固态合金的转变。
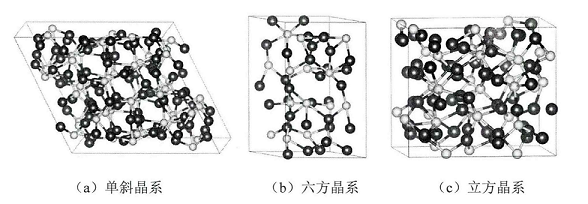
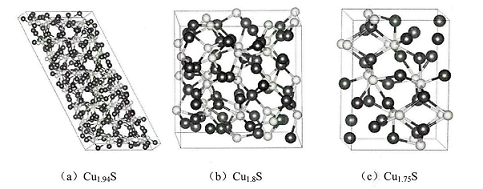
由于铜空位的存在,硫化亚铜也会以一些非整比化合物的形式存在,拥有多种化学计量比。到目前为止,从富铜的Cu2S晶体到贫铜的CuS晶体,CuXS(x=1 ~2)至少存在九种不同的相,其中至少有五种相能够在室温下稳定存在。在这些稳定相中,所有的CuXS(x=1 ~2)富铜相化合物都是P型半导体,例如常见的Cu2S (辉铜矿),Cu1.9S(久辉铜矿),Cu1.8S (方辉铜矿)和Cu1.75S (斜方蓝辉铜矿),其中非整合比CuxS的晶体结构如图1-2所示。
1、催化剂
纳米级Cu2S相比于普通的Cu2S具有特殊的小尺寸效应、表面效应等,还能自组装成不同的形貌,因而具有更多的特殊性能,例如,在光条件下可催化分解有机污染物,还可与金属结合生成混合物用于金属及金属氧化物的催化反应。Peng等 探究了不同实验条件下制备的纳米Cu2S (纳米颗粒、纳米线和纳米花)对 X-3B 染料的催化效果,以及催化效果与催化作用时间的关系,结果表明,自组装而成的纳米花催化效果最好(催化效率为 50.1% ),纳米颗粒的催化效果差(催化效率仅有 11.7% ),纳米线稍高于纳米颗粒(催化效率为20.3% )。催化作用的时间越长,纳米花的催化效果越好,而纳米颗粒与纳米线的催化效果则变化不大。 Zhao等采用溶剂热法制备出Cu2S微球和微环,并在室温下暴露在空气中的亚甲基蓝进行催化性能的研究。首先分别将样品分散在亚甲基蓝溶液中,黑暗条件下搅拌 1h,为了排除光照加热Cu2S的影响,将反应系统置于装有流动水的大玻璃容器中,然后在距离反应容器 20cm 处用 18W 的光照处理,并每隔 1h 检测亚甲基蓝的浓度。当催化 6h 后,微球催化系统剩余亚甲基蓝 30% ,而微环催化系统仅剩余 4% 的亚甲基蓝,所以微环的催化效率高于微球。Vinokurov 等用金属铑对Cu2S纳米晶体进行边缘修饰,制得了 Rh-Cu2S纳米笼颗粒,该产物由于其高效的催化性能和特殊的催化形式,被应用于金属和金属氧化物的催化。
2、太阳能电池
纳米Cu2S是一种重要的半导体材料,且具有较大的能带间隙,因此广泛应用于太阳能电池,如染料敏化太阳能电池、量子点敏化太阳能电池等。 Shuai 等在90℃ 时对 ZnO纳米管进行化学转化和阳离子交换合成了Cu2S纳米管,并用来作为染料敏化电池的辅助电极。在不同反应时间制备的Cu2S纳米管具有不同的光伏转化效率,随着反应时间的延长,光伏转化效率也逐渐提高(可达 2.88% )。Li等 制备了多孔Cu2S微球,对其光伏性能进行了测试,并与纳米颗粒的光伏性能进行了比较。首先将其制作成染料敏化电池极,装入已含有辅助电极的三明治型电池中,再浸入电解质溶液,然后在模拟太阳光照射的情况下通过电化学工作站测量光电流-电压曲线。结果表明:多孔微球的光电流密度可达1.38mA · cm-2 ,而纳米颗粒的光电流密度仅为0.85mA ·cm-2 ,因此从能量转化的角度来看,多孔微球更适合作为染料敏化电池的电极。 Gurpreet 等通过喷射热解沉淀过程制备出纳米Cu2S,并以此作为辅助电极来组装量子点敏化太阳能电池,利用太阳模拟器模拟太阳光( 100mW / cm -2 )测量电流 - 电压曲线,同时以硅标准电池作为校正,实验结果表明,光转化效率高达 3.75% ,光子 - 电流转化效率达 90% 。史继富等在最优条件下(盐酸的浓度为30% ,处理时间为 40min ,与多硫化钠反应的时间为 10s )制备出纳米Cu2S,并作为光阴极制作成量子点敏化太阳能电池,在太阳模拟器下测试其光电转化效率达 4.01% 。
2.3 其他应用
除了在催化剂和太阳能电池方面的广泛应用外,纳米Cu2S还可应用于锂离子电池、荧光标记、生物传感、场发射等方面。
1、 水热法
水热法通过反应釜提供高温、高压的环境,使化合物均匀地溶解在水中,从而有利于化学反应的进行,且矿化剂的使用可有效控制产物形貌。由该方法制得的产物具有良好的结晶形态,且不易团聚,有利于保持纳米材料的稳定性。水热法操作简单、产率高、污染少,是合成纳米材料的一种常用方法。
Zhang 等以Cu ( NO3 ) 2为铜源, CTAB (十六烷基三甲基溴化胺)为表面活性剂,加入到正戊醇-正己醇-水混合液中,在不断搅拌和超声处理下制得透明微乳液,再加入 DT(正十二硫醇),在水热条件下合成盘状纳米Cu2S。多组实验对比证明, DT为控制产物元素化学计量比和最终形貌的关键物质。Lv等采用水热法,以铜箔为铜源和基底,蒸馏水和乙二胺为共溶剂, CTAB为表面活性剂,再加入水合醋酸铜和硫脲,转移至高压釜中,160℃下反应10h,最后在铜箔两边分别得到Cu2S纳米片和六边形纳米盘。经表征表明, Cu2S纳米片的尺寸和厚度分别为 350~600nm 和15~25nm ,六边形纳米盘的边缘长度和厚度分别为 250~350nm和 150nm。 Yu等将铜箔、硫粉 (1mmol)、肼 ( 1mL )、CTAB ( 1mmol)、蒸馏水放入高压釜中, 180℃下反应 12h后,再将铜箔放入乙醇中超声处理,得到平均直径为110nm且具有较大长径比的Cu2S纳米线。为了探究纳米线的生长机理,他们还研究了不同实验条件对产物形貌的影响(,并提出Cu2S纳米线是通过收卷机理形成的。Song等采用水热法两步制得Cu2S纳米花,首先将 CuCl2 · 2H 2O ( 1g )、硫脲( 0.8g )、乙醇( 80mL )组成的悬浊液搅拌 0.5h ,转移至高压釜中, 160℃ 下反应6h得到Cu2S纳米片,然后再将纳米片加到由CuCl2 · 2H 2O ( 1g )硫脲( 0.2g )、乙醇( 80mL )组成的悬浊液中,相同水热条件下纳米片自组装成Cu2S纳米花。 Li等以CuCl2、[ BMIM ] SCN ( 1-丁基 -3- 甲基咪唑氰)、乙醇和水为原料,在高压釜中 180℃下反应 24h ,反应结束后,自然冷却至室温,过滤、洗涤、 60℃ 下真空干燥 10h ,得到纳米Cu2S多孔球。测试表明该形貌纳米Cu2S的能带宽度为 2.0eV 。他们还用相同的原料在 140℃下反应 24h 得到了 CuSCN 纳米花。
1.2、溶剂热法
溶剂热法是一种为弥补水热合成不适用于对水敏感材料的缺陷,而采用有机溶剂及有机溶剂和水混合物作为溶剂的方法,不仅扩大了水热法的合成范围,而且也能制备出更多类型的样品结构,但有机溶剂的使用会对环境带来负面影响。Wu等以CuSO4·5H2O和DMSO(二甲基亚砜)为原料,在高压釜中加热到 180℃ 反应 6~12h 后,洗涤、 60℃ 真空干燥 10h ,在没有模板和表面活性剂的情况下,得到双层折叠雪花片状 Cu2S树突。其中,DMSO 仅作为溶剂也是硫源和还原剂。 Li 等采用液相模板法合成了Cu2S纳米带,选择 CuCl 为铜源,以 Bi2 S3为模板和硫源,乙醇为溶剂,在高压釜中加热到120℃ ,并持续反应2d ,洗涤、真空干燥,得到Cu2S纳米带,经表征表明,纳米带的厚度和宽度分别20~80nm和 50~300nm 。Zhao等以CuCl为铜源,硫脲为硫源,乙醇和水混合液为溶剂, PVP (聚乙烯吡咯烷酮)为表面活性剂,置于高压釜中加热到 150℃ ,反应 5h 后,收集沉淀,洗涤、 55℃ 真空干燥,得到Cu2S层状微环和多孔微环。他们还探究了乙醇和蒸馏水体积比( R )、 PVP 和反应时间对产物形貌的影响,实验结果表明,微环是由更小的微球组装而成,且反应时间是影响组装过程的重要因素。 Gorai 等 以 Cu ( NO 3 )2 、硫脲为原料,乙二胺为溶剂,采用溶剂热法,在140℃下反应保温 4h 制备出花状Cu2S纳米树突,经表征表明,每个花瓣的长度为 3.0~4.5 μ m ,中心圆圈半径为 0.5~0.65 μ m ,且能从背面看出花瓣是由几片更小的叶子(长度为0.6~1 μ m )连接在主干上组成的。 Cao 等通过一锅式溶剂热过程,在不同实验条件下进行了多组实验,制备出尺寸和形状可控的Cu2S纳米颗粒。在对多组实验初步结果的后续处理中发现,无溶剂分散时制备出的 Cu2S颗粒具有原子级和粒子级水平的超晶格,又由于产物的尺寸、形状、结晶度具有可控性和溶液的多相共存性,使得原子级的超晶格存在自组装行为,这使其拥有更广的应用前景。 Li 等以水- 乙二醇混合液为溶剂,泡沫铜为反应模板,制备出Cu2S微米棒。首先将泡沫铜和硫粉加入到高压釜中,再加入乙二醇和去离子水,密封后加热到 160℃ , 24h 后将黑色产物放入二硫化碳中处理约 0.5h ,洗涤、 60℃ 干燥,最后得到Cu2S微米棒,经表征表明,微米棒的直径为 3~8 μ m ,长度为 80~150μ m 。 Li等采用溶剂热法,以CuC、硫脲为原料,合成多花状 Cu2S微米球。制备过程中,硫脲在 150℃下分解提供硫源, PVP 控制微米球的形成,经表征表明,微米球直径1.8 μ m ,且由纳米片组装而成。他们提出微米球的生长机理分为 3 个主要阶段:第一阶段,不规律聚集体生长成纳米粒或者纳米棒;第二阶段,不规律聚集体进一步转化为较长纳米。
[1]宋长青. Cu2S和VS2纳米结构制备及性能研究[D].华东师范大学,2014.
[2]许立信,王成,叶明富,陈国昌,储向峰,孔祥荣,XU Lixin,WANG Cheng,YE Mingfu,CHEN Guochang,CHU Xiangfeng,KONG Xiangrong- 《材料导报》2016年5期