
手机扫码访问本站

微信咨询
17(α)-17-乙酰基-17-羟基-雌甾-4-烯-3-酮(以下称为:孕诺酮) 是具有孕激素 活性的活性成分(例如,己酸孕诺酮和醋酸诺美孕酮)的合成中的重要的中间体。
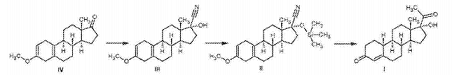
步骤1
(17α)-17-羟基-3-甲氧基雌甾-2,5(10)-二烯-17-甲腈的合成
在惰性气氛下,将50.0g的3-甲氧基雌甾-2,5(10)-二烯-17-酮混 悬在500ml乙醇 和34.25g氰化钾中,并在搅拌下加入0.15g的2,6-二 叔丁基-4-甲基苯酚。搅拌10分钟后, 用10分钟逐滴加入20.0ml乙酸。 将反应混合物从30-35℃温热至58-63℃,在该温度下搅拌 1小时,然后 冷却至20-25℃并搅拌16小时。向反应混合物中加入50ml水,将该浆 液搅拌1 小时,过滤出沉淀的晶体,用5×150ml的水混悬,再用2×100ml 的水洗涤。将湿的晶体在惰 性气氛下用300ml离子交换水搅拌15分钟, 过滤并用2×100ml的水洗涤。将湿的晶体用 75ml冷的乙醇和3×50ml 甲基叔丁基醚洗涤。收量:53.0g(96.9%),纯度(HPLC):97.49%。
1H NMR(DMSO-d6,500MHz)δ: 6.26(s,1H), 4.64(t,J=3.3Hz,1H), 3.45(s,3H), 2.70-2.87(m,1H), 2.49-2.63(m,2H), 2.37-2.49(m,1H), 2.22-2.34(m,1H), 1.97-2.08 (m, 1H), 1.76-1.96(m,3H), 1.61-1.75(m,4H), 1.51-1.60(m,1H), 1.37-1.47(m,1H), 1.24- 1.36(m,2H), 1.11-1.25(m,2H), 0.83(s,3H).
13C NMR(DMSO-d6,125MHz)δ:151.8, 127.3, 124.3, 121.8, 90.4, 76.5, 53.4, 48.9, 46.6, 44.3, 38.7, 37.4, 33.6, 29.8, 27.8, 26.9, 24.6, 22.9, 16.2。
步骤2
(17α)-3-甲氧基-17-[(三甲基甲硅烷基)-氧基]-雌甾-2,5(10)-二 烯-17-甲腈- 的合成
在惰性气氛下,向53.0g的(17α)-17-羟基-3-甲氧基雌甾 -2,5(10)-二烯-17-甲 腈、0.15g的2,6-二叔丁基-4-甲基苯酚和900ml 甲基叔丁基醚的搅拌混合物中,加入36.0g 咪唑在100ml四氢呋喃中的溶液。将反应混合物冷却到0-5℃,再以保持低于5℃的温度这 样的速率, 逐滴加入60.0ml三甲基氯硅烷。搅拌2小时后,向反应混合物中加入 50ml水,并 搅拌10分钟,然后将有机相分离并用3×50ml的水洗涤。将有机相用7.5g硫酸镁干燥,过滤,再将过滤出的干物质用2×25ml甲基叔丁基醚洗涤。将滤液浓缩至一半体积,在30-35 ℃下蒸馏除去3×300ml的甲基叔丁基醚,将溶液稀释至600ml,用于下一步骤。干物质含量:58.9g(90.4%),水含量:0.09g/100ml,纯度(HPLC):96.53%。
1H NMR(CD2Cl2,500MHz)δ:4.65(t,J=3.3Hz,1H), 3.50-3.57(m,3H), 2.80-2.95 (m,1H), 2.56-2.69(m,2H), 2.45-2.55(m,1H), 2.33-2.41(m,1H), 2.09(br.s.,1H), 2.01 (ddd,J=14.8,9.2,5.6Hz,1H), 1.95(dd,J=13.3,2.8Hz,1H), 1.90(dd,J=6.4,0.7 Hz, 1H), 1.76-1.84(m,1H), 1.60-1.76(m,4H), 1.49-1.55(m,1H), 1.33-1.44(m,2H), 1.20- 1.32(m,2H), 0.92(s,3H), 0.25(s,9H)。
13C NMR(CD2Cl2,125MHz)δ:153.1, 128.1, 125.4, 121.6, 91.0, 79.4, 54.2, 51.0, 47.6, 45.3, 40.0, 39.5, 34.6, 31.0, 30.8, 28.8, 27.9, 25.8, 24.0, 16.7, 1.3。
步骤3
(17α)-17-乙酰基-17-羟基-雌甾-4-烯-3-酮的合成
将(17α)-3-甲氧基-17-[(三甲基甲硅烷基)-氧基]-雌甾-2,5(10)- 二烯-17-甲 腈在600ml甲基叔丁基醚的溶液在搅拌下冷却至-40℃,然后 以保持低于-30℃的温度这样 的速率,加入80ml的N,N,N′,N′-四甲基乙 二胺和180ml甲基锂溶液(3M,在二乙氧基甲烷 中),将该反应混合物 在该温度下搅拌1小时,然后倒入通过强力冷却而冷却到-15~(-10) ℃ 的1000ml的4N盐酸溶液中,将反应混合物在20-25℃下搅拌16小时, 然后通过加入约 800ml的3M乙酸钠而将溶液的pH调节至4~5。蒸馏除 去挥发性有机成分,将残留物在20~ 25℃下搅拌1小时,过滤出沉淀的粗产物,将其混悬于5×500ml水中,用100ml冷的甲醇洗涤,并在真空烘箱中干燥。收量:32.42g(67.1%),纯度(HPLC):89.66%
在惰性气氛下,在60℃下将32.42g粗产物加入到97ml甲醇中,在得到透明溶液后,将所得混合物冷却到20-25℃。用2~3分钟将16.2ml 水加入到搅拌的浆液中,然后将其 冷却到至0-5℃。搅拌1小时后,过滤出晶体,混悬于11.2ml水和67.1ml甲醇的混合物中,然 后在真空烘 箱中干燥。收量:25.67g(79.2%),纯度(HPLC):98.47%
1H NMR(CDCl3,800MHz)δ: 5.82-5.85(m,1H), 2.85(s,1H), 2.69(ddd,J=14.9,11.5,3.1Hz,1H), 2.47-2.51(m,1H), 2.39-2.43(m,1H), 2.28(s,3H), 2.23-2.31(m,3H), 2.06-2.11(m,1H), 1.89-1.93(m,1H), 1.81-1.88(m,2H), 1.72-1.80(m,2H), 1.61(ddd, J= 15.2,9.2,6.3Hz,1H), 1.52-1.58(m,1H), 1.35-1.44(m,3H), 1.22-1.29(m,1H), 1.12-1.18 (m,1H), 0.90(dtd,J=12.0,10.6,4.2Hz,1H), 0.78(s,3H)。
13C NMR(CDCl3,201MHz)δ:211.6, 199.9, 166.4, 124.6, 89.8, 49.2, 49.0, 48.4, 42.4, 40.2, 36.5, 35.5, 33.5, 31.1, 30.0, 27.9, 26.6, 25.9, 23.8, 15.5。
[1]CN201480068436.2 19-去甲孕甾-4-烯-3,20-二酮-17α-醇(孕诺酮)的制备方法及其中间体